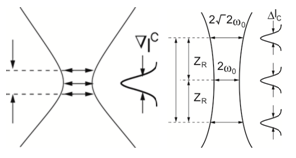
図1:焦点深度と光学系のNA
図1は、焦点におけるスポットサイズとDOFとの関係を高NAと低NAにおいて示したものである。
一般的にOCTは低NAの光学系を用いて、長いDOFの下で動作させる。この場合、共焦点パラメタはコヒーレンス長より大きくなる(b > Δz)。そして、奥行き分解能は光の遅延時間測定の結果に支配され、先ほどの奥行き分解能の式によってOCTの奥行き分解能は決められる。顕微鏡と比較すると、OCTはNAに依存しない奥行き分解能を実現することができる。この特性は、測定対象と光学系との距離を長く取らなければならないような眼科応用などに対して非常に有効である。しかし、低NAは横方向分解能を制限するため、露光焦点は大きくなってしまう。
一方で、OCTにおいても高NAを採用して横方向分解能を高く設定することもできる。しかし、この設定ではDOFを制限してしまう。また、この設定は顕微鏡や共焦点顕微鏡において採用される設定であり、奥行き分解能においてもOCTの優位性が制限される。もし、より高い横方向分解能なイメージを必要とする場合、en-face画像を構築することが有効である。
さらに、高NAを採用すると共焦点パラメータとなる条件(b<Δz)まで光を集光することができる。このような条件では、共焦点とコヒーレンスゲートを併せ持った信号処理が可能であり、異なる場所から後方散乱もしくは後方反射した信号を識別するために使われる。このようなモードを主にOptical coherence microscopy(OCM)と呼ぶ。
また、近年Full-field OCTという新しい技術が開発され、Linnik干渉計とCCDカメラを使ったコヒーレンスゲート検出法による高分解能はen-faceイメージを実現した。
以上の説明のように、OCTにおける横方向分解能とDOFとにはトレードオフが存在し、初期のOCTの研究では奥行き分解能の向上に注目が集まっていた。当時の医療用OCTの奥行き分解能は10~15 μm程度であった。しかし、最新のOCTシステムでは、内視鏡やカテーテル画像に対しては5 μm以下であり、眼科応用では2~3 μmを実現している。奥行き分解能の改善は、主にスーパールミネッセントダイオードやレーザー光源の進展によってなされてきた。
無料ユーザー登録
登録することで3000以上ある記事全てを無料でご覧頂けます。
- @optipedia.info ドメインより登録の手続きを行うためのメールをお送りします。受信拒否設定をされている場合は、あらかじめ解除をお願いします。
- Gmailをお使いの方でメールが届かない場合は、Google Drive、Gmail、Googleフォトで保存容量が上限に達しているとメールの受信ができなくなります。空き容量をご確認ください。