さらなる新波長を求めるトレンドに応える、フローサイトメトリーレーザ
さらなる個別化医療に対するニーズが高まる中で、新しいレーザ波長と、複数の波長が統合されたレーザライトエンジンが、高い性能を備える高次元アナライザの実現につながることが、研究者らによって見出されている。
長期化する新型コロナウイルス感染症(COVID-19)のパンデミックによって、個別化医療に向けた動きが一層促進されており、それによって、研究と臨床の両方の分野を対象とした、さらに高度なフローサイトメトリー装置の必要性が高まっている。具体的には、いわゆる高次元、または、マルチパラメータのフローサイトメトリーにおいて、より大きなデータセットを提供するためにより多くのレーザ波長を使用することにより、より多くの異なる種類の細胞を単一の装置で測定することが求められている。レーザメーカーは現在、UV、可視域、近赤外域(NIR)の新しい波長と、メーカーによる装置開発を効率化する、マルチ波長のレーザライトエンジンによって、この要求に対応している。
フローサイトメトリーの基礎
フローサイトメーターは、血液サンプル中のさまざまな種類の細胞の数を数えることのできる装置である。血液サンプルを最初に凝集し、複数の蛍光色素の混合物でそれを処理することにより、これが行われる。蛍光色素とは、標的とする細胞表面上の特定のタンパク質にそれぞれ選択的に結合する、蛍光化学物質である。処理後に細胞は装
置に注入され、1つずつ1列に並んだ1つのフローストリームとしてレーザ相互作用ゾーンに供給される。複数の異なる波長のレーザビームをこのストリームに照射することにより(図 1)、蛍光と光散乱が生じる。各蛍光色素はそれぞれ異なる波長で蛍光を発するため、それによって個々の細胞を識別することができる。
光学系はバンドパスフィルタを使用することにより、蛍光信号を収集して波長ビンに分類する。光信号は、検出器(光電子増倍管[photomultiplier tube:PMT]、または、アバランシェフォトダイオード[APD])によって、定量的に測定される。
臨床用装置では一般的に、最大4つのレーザ波長と最大10個の検出器が使用される。最新の研究用装置では、最大9つのレーザ波長と60個の検出器が使用される。どちらの種類の装置も高速で、一般的に1秒あたり数百個の細胞を分析することができる。
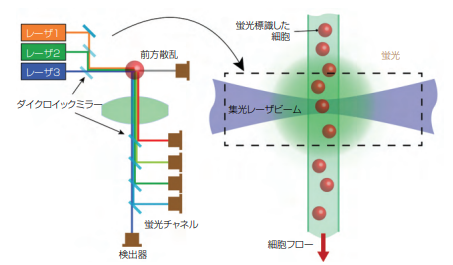
図1 フローサイトメトリーでは、1つずつ1列に並んで、細長いフローストリームとして通過する細胞が、1つ以上のレーザビームによって励起される。
高次元サイトメトリーの課題
蛍光信号は必ず、レーザ励起波長よりも長い(ストークスシフトされた)波長に存在する(図 2)。このシフトにより、バンドパスフィルタとカットオフフィルタの組み合わせを使用して、蛍光を散乱レーザ光から効率的に分離することができる。理論的な最大信号雑音比(S/N比)は、励起曲線のピークで蛍光色素を励起し、その蛍光をできるだけ多く検出することにより、達成される。
マルチパラメータフローサイトメトリーの任意のアプリケーションにおいて、試薬パネルは、すべてが異なる励起及び蛍光スペクトルを持つように慎重に選択された、複数の蛍光色素で構成される。これは、装置が信号を分離して、それによって、各蛍光色素が各細胞にどれだけ結合しているかを判定できるようにするために、非常に重要
である。それができれば、その装置によって細胞の種類を明確に判定することができる。
ここでの課題は、励起と蛍光の両方の発光スペクトルが、かなり幅広で裾野が長いために、いくらかのクロストークが避けられないことである。また、特定のタンパク質をどれだけ発現するかについては、細胞の種類によって自然なばらつきが存在する。装置設計者や、試薬パネルを設計するエンジニア/科学者は、クロストークに加えて、最終データの変動係数(Coefficient of Variation:CV)を最小限に抑える必要がある。
一般的に採用されている方法(図2)は、励起波長と蛍光検出ウィンドウを交互に配置するというものである。各検出ウィンドウ内の信号は、「散布図」を生成するように、互いに対してプロットされる。既知と新規の両方の種類の細胞の検出を目的とした研究アプリケーションでは、プロットが手作業で作成されることがよくある。臨床実験では、検査量が多いためにこのような監視型の分析は非実用的で、代わりに多変量コンピュータ解析が、各細胞の種類の自動判別に使用される。
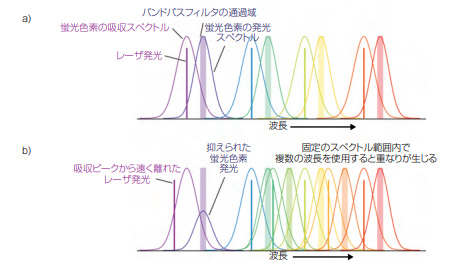
図2 各レーザ波長が、蛍光色素の吸収ピークに近ければ、最大の蛍光発光が得られるため、理想的である。また、レーザ波長と蛍光ピークが十分に離れていれば、バンドパスフィルタによって両者を分離することができる (a)。実際のシステムでは、蛍光色素の吸収ピークから離れた波長で発光するレーザが使われるために、発光が低下する場合がある。また、特定のスペクトル範囲内でより多くのレーザを使おうとすると、励起と発光の間にかなりの重なりが生じ、信号の分解は難しくなる (b)。
(もっと読む場合は出典元へ)
出典元
http://ex-press.jp/wp-content/uploads/2022/05/032-034_bioft_flow_cytometry.pdf